Nutriënten als munitie voor de afweercompetentie

Robert van Esch MSc.
PsychoNeuroImmunoloog
Ons immuunsysteem bestaat uit drie verdedigingslinies, namelijk de anatomische en fysiologische barrières, de aangeboren of aspecifieke afweer en de adaptieve of specifieke afweer. De primaire barrières worden opgeworpen door epitheellagen, membranen, mucosa, vochtreservoirs en microbiota. Het aspecifieke immuunsysteem bestaat uit cellen en complementfactoren zonder geheugencapaciteit. Het specifieke immuunsysteem kenmerkt zich door een cellulaire en humorale component met een robuust, immunologisch geheugen, cytokine- en antilichaamproductie. Zowel bij zijn competentie als ontstekingsgerichtheid is het totale immuunsysteem mede afhankelijk van de beschikbaarheid en endogene aanwezigheid van essentiële voedingsstoffen of nutriënten.
Een adaptief en interactief immuunsysteem ligt aan de basis voor het oplossen van ontstekingsprocessen. Tevens zijn de intacte status van de fysieke en fysiologische barrières van het lichaam van belang voor het optimaal functioneren van het immuunsysteem. Een acute ontstekingsrespons is van nature tijdgebonden. Vanaf de start van het ontstekingsproces wordt, onder normale fysiologische condities, na ongeveer twaalf uur de hoogste activiteit van betrokken afweercellen bereikt. Die ontstekingsreactie gaat gepaard met pijn en koorts en behoort maximaal zes dagen te duren. Het afremmen, stabiliseren en beëindigen van de ontsteking gebeurt door middel van een gecoördineerde interactie tussen pro- en anti-inflammatoire moleculen, die al na twaalf uur geïnitieerd wordt en die leidt tot de omzetting van eicosanoïden, waarbij ontstekingsremmende prostaglandinen, zoals lipoxinen, resolvinen en protectinen, dominant worden. Diverse pathofysiologische factoren kunnen dat proces echter verstoren, waardoor immunologische overactiviteit ontstaat en de herstelfase wordt ingeruild voor chronische ontstekingen en toename van weefselschade.
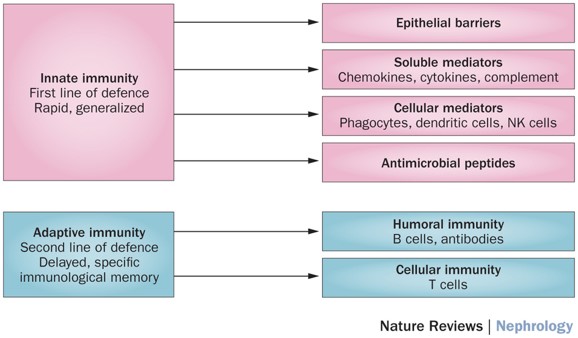
Afweercompetentie
Zowel het op gang brengen van de onstekingsfase als het beëindigen van de ontstekingsrespons hangen samen met de individuele afweercompetentie. Deze competentie staat voor de potentie of bekwaamheid van het eigen immuunsysteem om adequaat te kunnen reageren op een antigene stimulatie en een toereikende respons te kunnen produceren. Die afweercompetentie hangt nauw samen met de nutriëntenstatus. Een optimale voedingsstatus is fundamenteel bij modulatie van ontstekingen en oxidatieve stress, die samengaan met immunologische activiteit. De consumptie van proteïnen met een hoge biologische waarde is bijvoorbeeld noodzakelijk voor optimale productie van antilichamen. Zo is het semi-essentiële aminozuur glutamine nodig voor de expressie van diverse genen die betrekking hebben het immuunsysteem. Ten eerste ondersteunt glutamine endotheelcellen bij handhaving van de intestinale barrièrefunctie en is het een precursor voor de belangrijkste lichaamseigen antioxidant glutathion. Voorts is glutamine een energiesubstraat voor macrofagen, neutrofielen en lymfocyten bij hun proliferatie en betrokkenheid bij weefselreparatie. Tevens induceert het aminozuur de expressie van heat shock proteins (HSP). HSP spelen onder meer een rol bij weefselbescherming na fysiologische stress. Hun verminderde activiteit kan leiden tot toename van cellulaire schade en apoptose. Bij mensen is waargenomen dat verminderde beschikbaarheid van proteïnen, zoals glutamine, kan leiden tot verhoogde vatbaarheid voor virale infecties, verminderde functionaliteit van neutrofielen en het complement systeem en verminderde reactiviteit van antilichamen.
Resoleomics
Net als bij proteïnen het geval is, zijn vetzuren eveneens van betekenis voor het goed functioneren van de immunologische linies. Bovenal spelen vetzuren een prominente rol bij het oplossen van ontstekingsprocessen. Het zelf-oplossend vermogen van een ontstekingsrespons wordt resoleomics genoemd en wordt ten uitvoer gebracht en gecontroleerd door het aangeboren immuunsysteem en gereguleerd door het sympathische zenuwstelsel en de bijnierhormoon-as (HPA-as). Hierbij worden metabolieten gebruikt afkomstig van de onverzadigde vetzuren arachidonzuur (AA), eicosapentaeenzuur (EPA) en docosahexaeenzuur (DHA). Die metabolieten worden eicosanoïden genoemd. Pro-inflammatoire eicosanoïden, waaronder leukotriënen en prostaglandinen, initiëren de ontstekingsreactie met AA middels enzymatische tussenkomst van lipoxygenase-5 (LOX) en cyclo-oxygenase-2 (COX). Specifieke neutrofielen stimuleren vervolgens de omzetting richting anti-inflammatoire eicosanoïden, waaronder lipoxinen, door enerzijds de productie van LOX-5 af te remmen en anderzijds de activiteit van LOX-12 en LOX-15 en acetylatie van COX-2 te stimuleren. De productie van ontstekingsremmende lipoxinen uit AA en resolvines, protectines en marines uit respectievelijke EPA en DHA initiëren tenslotte de terminatiefase, waarin de ontstekingsreactie wordt gestopt. Bijgevolg worden ook de werkzaamheid van neutrofielen, cytotoxische afweercellen, macrofagen en pro-inflammatoire transcriptiefactoren afgeremd. Op systemisch niveau ondersteunen boodschappermoleculen afkomstig van het sympathische zenuwstelsel de initiatie van de pro-inflammatoire ontstekingsrespons, die vervolgens in toenemende kracht wordt afgeremd door cortisol afkomstig van de HPA-as gedurende de resolutie- en terminatiefase.
Zowel op lokaal als op systemisch niveau is de verhouding tussen de vetzuren AA, EPA en DHA van invloed op de fasering en het verloop van de ontstekingsrespons. Met name gebrek aan de omega-3 vetzuren EPA en DHA kan een ongunstige verloop of verlenging van de ontstekingsfase tot stand brengen. De aanwezigheid van de vet oplosbare vitaminen A (retinol) en D is eveneens van invloed op het verloop van onstekingsprocessen. Zij fungeren, evenals omega-3 vetzuren, als resolvents ofwel ontsteking oplossende moleculen.
A en D
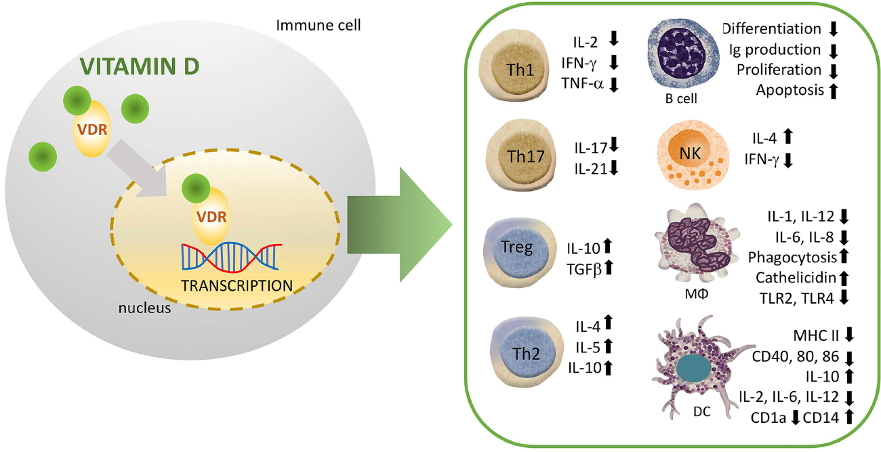
Net als EPA en DHA beïnvloeden vitamine A en het actieve vitamine D3 (1,25-dihydroxycholecalciferol) genen door aanhechting aan specifieke DNA-receptoren. De drie actieve vormen van vitamine A (retinal, retinol en retinoïdezuur) beïnvloeden diverse fysiologische functies, waaronder handhaving van epitheelbarrières en de afweermodulatie. Zo stimuleert retinoïdezuur in intestinale weefsels specifieke receptoren van B- en T-lymfocyten, die weefselspecifiek gericht zijn, opdat in de darmen een adequate balans kan worden gehandhaafd tussen immuniteit en tolerantie. Voorts bepaald vitamine A mede de embryonale en postnatale inductie van lymfatische cellen. Ook is de vitamine essentieel bij de activatie en differentiatie van T-cellen naar T-helpercellen. Bovendien staat het aantal circulerende T-regulatiecellen (Treg) mede onder invloed van de beschikbare hoeveelheid A en D. Met name vitamine D heeft impact op zowel het aantal als de functionaliteit van de Treg in circulatie. Uit diverse studies bij mensen is gebleken dat 3 tot 12 maanden suppletie met vitamine D kan leiden tot toename van het aantal circulerende Treg. Tevens beïnvloedt vitamine D de diverse T-helpercellen via de aanwezigheid van D-gevoelige receptoren. Uit onderzoek is gebleken dat zowel de verhoogde aanwezigheid van vitamine D als activatie van de receptor van vitamine D kan leiden tot modulatie van de ontwikkeling en functionaliteit van T-helpercellen type 1 ten gunste van T-cellen type 2 en type 17. Dit leidt vervolgens tot verminderde aanwezigheid en activiteit van ontstekingseiwitten en bijbehorende transcriptiefactoren. Daarnaast stimuleert het pro-hormoon de antimicrobiële immuunrespons van cellen uit het aangeboren afweersysteem tegen bacteriën, virussen en schimmels. Bij de aanwezigheid van fysiologische hoeveelheden 1,25(OH)D3 kunnen monocyten prolifereren en promoot het de macrofagencapaciteit voor chemotaxis en fagocytose. Ook kan 1,25(OH)D3 de productiecapaciteit induceren van antimicrobiële peptiden in monocyten, neutrofielen en epitheelcellen. Vitamine D3 als 25-hydroxycholecalciferol 25(OH)D3, zoals gebruikt in supplementen, is het belangrijkste vitamine D metaboliet in het bloed en kent een halfwaardetijd van 15 dagen, terwijl het actieve 1,25(OH)D3 een halfwaardetijd heeft die in uren wordt gemeten. De serumwaarde van 25(OH)D3 wordt derhalve als beste indicator gezien voor de biologische beschikbaarheid van vitamine D3.
Zink en selenium
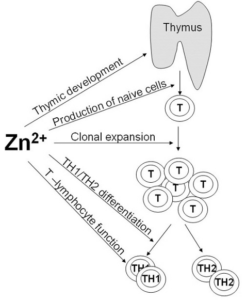
Afweermodulatie hangt nauw samen met de afweercompetentie van zowel het aangeboren als verworven immuunsysteem en is mede afhankelijk van specifieke micronutriënten. Met name zink en selenium zijn hierbij van cruciaal belang. Zink is benodigd voor de normale ontwikkeling en functie van cellen die het aangeboren immuunsysteem vertegenwoordigen, alsook neutrofielen en natural killer-cellen (NK). Tevens beïnvloedt zink de groei en functie van T- en B-lymfocyten. Gebrek aan zink heeft een negatieve impact op de ontwikkeling en functionaliteit van afweercellen bij zowel aangeboren als verworven immuniteit. Primaire manifestaties hiervan kunnen zijn: thymusinvolutie, een verminderd aantal T-helpercel type 1 en afgenomen activiteit van lymfocyten, NK, macrofagen en neutrofielen.
Uit diverse studies bij dieren en mensen blijkt dat zinkdeficiëntie kan leiden tot lagere zinkconcentraties in lymfocyten, granulocyten en macrofagen en verhoogde kenmerken van oxidatieve stress. Bovendien kan zinktekort leiden tot lagere serumspiegels van thymuline. Thymuline is een thymushormoon dat, voor expressie van de biologische activiteit, afhankelijk is van zink. Thymuline bindt zich aan specifieke receptoren op T-cellen en stimuleert zo de functionaliteit, waaronder de cytotoxiciteit, immunologische suppressie en productie van cytokinen, zoals IL-2 en IFN-γ. Suppletie met zink in vivo en in vitro kan aantoonbaar de spiegel en activiteit van thymuline verbeteren bij zinkdeficiëntie. Uit studies bij mensen zijn de voordelen aangetoond van zinksuppletie bij infectieziekten. Middels dubbelblinde en placebo gecontroleerde testen (RCT) stelde men vast dat dagelijks toediening met 10 milligram elementair zink gedurende drie maanden de incidentie en duur van acute en chronische diarree en acute infecties van de diepere luchtwegen bij pasgeborenen en jonge kinderen doet verminderen. Daarnaast werd bij mensen met sikkelcelanemie middels een placebo gecontroleerde studie waargenomen dat longontsteking, tonsillitis, urineweginfecties door pathogene bacteriën minder vaak voorkwamen na zinksuppletie met hoge doses. Ook bij senioren is zinksuppletie effectief gebleken als ondersteuning van de afweercompetentie.
Bij een RCT met 50 gezonde personen ouder dan 55 jaar werd gedurende twaalf maanden orale suppletie toegepast met 45 milligram elementair zink als gluconaat. Hun status bij aanvang werd vergeleken met die van jongvolwassenen, waarbij men vaststelde dat de onderzoeksgroep lagere plasmaspiegels had van zink en ex vivo meer aanwezigheid van ongunstige cytokinen, meer fysiologische kenmerken van oxidatieve stress en endotheelceladhesiemoleculen. Aan het eind van de studieduur werd waargenomen dat bij de testgroep die zinksuppletie had gekregen niet alleen hogere plasmaspiegels van zink werden geconstateerd, maar ook een significant lagere incidentie van infectie en minder ex vivo manifestatie van TNF-α en oxidatieve stress waarneembaar waren ten opzichte van de placebogroep. Middels empirische bevindingen mogen we vaststellen dat het langdurig gebruik van hoge doses zink zonder nulmeting kan leiden tot intracellulaire zinkaccumulatie en intracellulaire deficiëntie van koper. Verantwoorde interventies met langdurige zinksuppletie behoren aldus gepaard te gaan met de ratiobepaling van de intracellulaire zink- en koperstatus.
Net als zink heeft ook selenium impact op de specifieke afweercompetentie. Uit onderzoek is gebleken dat seleniumdeficiëntie kan bijdragen aan immunologische incompetentie met verhoogde vatbaarheid voor infectie en mogelijk zelfs carcinogene processen tot gevolg. Bij zoogdieren is selenium actief als onderdeel van selenoproteïnen. Bij de mens zijn 25 selenoproteïnen actief. De meeste fungeren als enzymen in redoxreacties en enkele functioneren als non-enzymatische factoren in de stofwisseling. Opvallende afweer gerelateerde selenoproteïnen zijn de glutathionperoxidasen, selenofosfaat synthetase en selenoproteïne K.
Seleniumsuppletie veroorzaakt grotendeels afweerstimulatie bij het cellulaire en niet bij het humorale deel van het immuunsysteem, wat zich onder andere kan manifesteren als T-celproliferatie, NK-activiteit en toegenomen functionaliteit van het aangeboren immuunsysteem. Zo worden macrofagen door seleniumspiegels beïnvloed in hun ontstekingssignalering-capaciteit en anti-pathogene activiteit. Daarbij is vastgesteld dat selenium een fenotypische verschuiving induceert bij macrofagen van een pro-inflammatoire naar een anti-inflammatoire modus. Daarnaast kunnen sommige selenoproteïnen vanwege hun anti-oxidatieve eigenschappen bijdragen aan stimulering van de antivirale immuniteit.
Het belang van toereikende inname van selenium en de incorporatie hiervan in de selenoproteïnen, die specifiek betrokken zijn bij de immuunrespons, is aangetoond bij onderzoek op celculturen en bij in vivo onderzoek op dieren en mensen. Seleniumdeficiëntie en onderdrukte expressie van selenoproteïnen kunnen van betekenis zijn bij de toegenomen manifestatie van ontstekingsbevorderende cytokinen in diverse weefsels, zoals maag-darmstelsel, uterus en borstklieren. Tegelijkertijd kan de sufficiënte inname van selenium mogelijk leiden tot een toename van specifieke ontstekingsprocessen. Bij een studie met astmatische muizen werd bijvoorbeeld waargenomen dat seleniumdeficiëntie zorgde voor verminderde luchtwegontsteking. De toename van seleniuminname leidde tot meer ontsteking, die echter weer afnam toen de muizen therapeutische hoeveelheden kregen toegediend. Uit een ex vivo studie met humane cellen bleek voorts dat inname van seleniumrijke voeding leidde tot de verhoogde activiteit van leukocyten in de bloedcirculatie. Ook ontdekte men bij volwassenen met een marginale seleniumstatus dat suppletie met selenium, soms in combinatie met zink, zorgde voor een betere vaccinatierespons tegen het influenza- en poliovirus. Bij patiënten met Acute Respiratory Distress Syndrome bleek de intraveneuze toediening met selenium te zorgen voor herstel van de anti-oxidatieve capaciteit van de longen, waardoor de ontstekingsrespons werd afgeremd en de ademhalingsfunctie verbeterde. De meest overtuigende bevindingen betreffende de rol van selenium bij de antivirale immuniteit hebben betrekking op HIV-infectie, die wereldwijd vooral personen treft met inadequate voedselvoorziening. Verminderde seleniuminname wordt tevens geassocieerd met de prevalentie van HIV en de status van het aantal T-helpercellen correleert met de seleniumstatus bij positief geteste HIV-patiënten. Uit enkele populatiestudies bleek bovendien een associatie tussen seleniumgebrek een toename van sterfte aan AIDS. Uit een RCT blijkt dat suppletie met selenium de hospitalisatie en sterfte door chronische diarree bij HIV-patiënten sterk kan verminderen en hun aantal T-helpercellen kan verbeteren. Opvallend is dat de studieresultaten mede afhankelijk kunnen zijn van de context van de seleniumsuppletie. Zowel de vorm als dosering blijken namelijk van invloed op het eindresultaat. Zo constateerden wetenschappers aan de hand van een RCT met diverse vormen en doseringen van selenium dat de door gist verrijkte vorm in een dagelijkse dosis van 100 tot 200 microgram elementair selenium, het meest effectief bleek bij immunisatie na influenzavaccinatie.
Conclusies
Aan de hand van wetenschappelijk onderzoek constateert men dat voeding, die toereikende hoeveelheden bevat van micronutriënten en omega-vetten, een positieve impact kan hebben op de afweerfunctie. Opvallende, essentiële micronutriënten die de wetenschappelijke toets kunnen doorstaan als munitie voor de afweercompetentie zijn met name vitamine A en D, selenium en zink. Ook andere nutriënten, zoals glutamine en omega-3 vetzuren kunnen van betekenis zijn bij het optimaal laten functioneren van ons immuunsysteem. Zowel bij ontstekingsziekten als bij infecties kan het bepalen van de individuele status van betreffende micronutriënten zinvol zijn om gerichte therapeutische interventies te overwegen.
Wu D, Lewis ED, Pae M and Meydani SN. Nutritional Modulation of Immune Function: Analysis of Evidence, Mechanisms and Clinical Relevance. Front. Immunol. 9(3160), 2019
Iddir M et al. Strengthening the Immune System and Reducing Inflammation and Oxidative Stress through Diet and Nutrition: Considerations during the COVID-19 Crisis. Nutrients 12(1562), 2020
Ah, O. Protein Energy Malnutrition and Susceptibility to Viral Infections as Zika and Influenza Viruses. Nutr. Food Sci 6(2), 2016
Kim H. Glutamine as an Immunonutrient. Yonsei Med J 52(6): 892-897, 2011
Bosma-den Boer et al. Chronic inflammatory diseases are stimulated by current lifestyle: how diet, stress levels and medication prevent our body from recovering. Nutrition & Metabolism 9(32), 2012
Bono MR et al. Retinoic Acid as a Modulator of T Cell Immunity. Nutrients 8(349), 2016
Fisher SA, Rahimzadeh M, Brierley C, Gration B, Doree C, Kimber CE. The role of vitamin D in increasing circulating T regulatory cell numbers and modulating T regulatory cell phenotypes in patients with inflammatory disease or in healthy volunteers: A systematic review. PLoS ONE 14(9), 2019
Cantorna MT et al. Vitamin D status, 1,25-dihydroxyvitamin D3 and the immune system. Am J Clin Nutr 80: 1717–1720, 2004
Prasad AS. Zinc in Human Health: Effect of Zinc on Immune Cells. MolMed 14(5-6): 353-357, 2008
Sazawal S et al. Zinc supplementation reduces the incidence of acute lower respiratory infections in infants and preschool children: a double blind controlled trials. Pediatrics. 102: 1–5, 1998
Prasad AS et al. Zinc supplementation decreases incidence of infections in the elderly: effect of zinc on generation of cytokines and oxidative stress. Am J Clin Nutr 85: 837– 844, 2007
Avery JC and Hoffmann PR. Selenium, Selenoproteins, and Immunity. Nutrients 10(1203), 2018
Ivory K et al. Selenium supplementation has beneficial and detrimental effects on immunity to influenza vaccine in older adults. Clinical Nutrition 36: 407-415, 2017


